TERMODINAMICA
Proceso isobárico
Un proceso isobárico es un proceso termodi que ocurre a presión constante. La Primera Ley de la Termodinámica, para este caso, queda expresada como sigue:
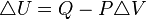
Proceso isotérmico
Se denomina proceso isotérmico o proceso isotermo al cambio reversible en un sistema termodinámico, siendo dicho cambio a temperatura constante en todo el sistema. La compresión o expansión de un gas ideal puede llevarse a cabo colocando el gas en contacto térmico con otro sistema de Capacidad calorífica muy grande y a la misma temperatura que el gas; este otro sistema se conoce como foco calórico. De esta manera, el calor se transfiere muy lentamente, permitiendo que el gas se expanda realizando trabajo. Como la energía interna
de un gas ideal sólo depende de la temperatura y ésta permanece
constante en la expansión isoterma, el calor tomado del foco es igual al
trabajo realizado por el gas: Q = W.
Una curva isoterma es una línea que sobre un diagrama
representa los valores sucesivos de las diversas variables de un
sistema en un proceso isotermo. Las isotermas de un gas ideal en un diagrama P-V, llamado diagrama de Clapeyron, son hipérbolas equiláteras, cuya ecuación es P•V = constante.
Proceso adiabático
En termodinámica se designa como proceso adiabático a aquél en el cual el sistema (generalmente, un fluido que realiza un trabajo) no intercambia calor con su entorno. Un proceso adiabático que es además reversible se conoce como proceso isoentrópico. El extremo opuesto, en el que tiene lugar la máxima transferencia de calor, causando que la temperatura permanezca constante, se denomina proceso isotérmico.
El término adiabático hace referencia a elementos que impiden la transferencia de calor
con el entorno. Una pared aislada se aproxima bastante a un límite
adiabático. Otro ejemplo es la temperatura adiabática de llama, que es
la temperatura que podría alcanzar una llama si no hubiera pérdida de
calor hacia el entorno. En climatización los procesos de humectación
(aporte de vapor de agua)
son adiabáticos, puesto que no hay transferencia de calor, a pesar que
se consiga variar la temperatura del aire y su humedad relativa.
El calentamiento y enfriamiento adiabático son procesos que comúnmente ocurren debido al cambio en la presión de un gas. Esto puede ser cuantificado usando la ley de los gases ideales.
En otras palabras se considera proceso adiabático a un sistema
especial en el cual no se pierde ni tampoco se gana energía calorífica.
Esto viene definido según la primera ley de termodinámica describiendo
que Q=0
Si se relaciona
Proceso isocórico
Un proceso isocórico, también llamado proceso isométrico o isovolumétrico es un proceso termodinámico en el cual el volumen permanece constante;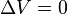 . Esto implica que el proceso no realiza trabajo presión-volumen, ya que éste se define como:
. Esto implica que el proceso no realiza trabajo presión-volumen, ya que éste se define como: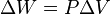 ,
,
Ciclo de Carnot
El ciclo de Carnot se produce cuando un equipo que trabaja absorbiendo una cantidad de calor Q1 de la fuente de alta temperatura, cede un calor Q2 a la de baja temperatura produciendo un trabajo sobre el exterior. El rendimiento viene definido por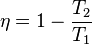




No hay comentarios.:
Publicar un comentario